توجه: این یک مقاله علمی در مورد گال است، چنانچه نیازمند اطلاعات عمومی در مورد بیماری گال هستید، مطالعه مقاله ” گال چیست؟ ” پیشنهاد میشود.
مقدمه
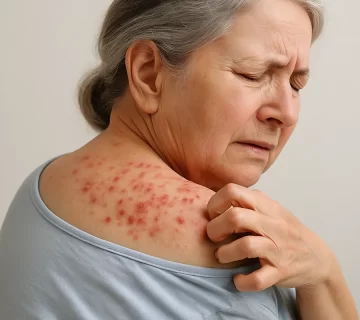
گال یا اسکابیس، یک بیماری پوستی انگلی مسری است که عامل ایجاد آن کنه میکروسکوپی Sarcoptes scabiei var. hominis میباشد. این انگل از طریق تماس نزدیک پوست به پوست بین انسانها منتقل میشود و در لایههای سطحی اپیدرم انسان لانهگزینی میکند. گال معمولاً با خارش شدید، بهویژه در شب، و بروز ضایعات پوستی در نقاط خاصی از بدن همراه است. این بیماری از دیرباز در جوامع انسانی وجود داشته و علیرغم پیشرفتهای علمی، هنوز هم در بسیاری از مناطق جهان، بهویژه در جوامع پرجمعیت، محروم و با سطح بهداشت پایین، بهعنوان یک مشکل بهداشتی مهم مطرح است.
در سالهای اخیر، سازمان جهانی بهداشت (WHO) گال را در فهرست بیماریهای گرمسیری نادیدهگرفتهشده (Neglected Tropical Diseases) قرار داده است. این تصمیم بر اهمیت فزاینده این بیماری در سلامت عمومی جهانی تأکید دارد. گال، بهویژه در صورت بروز نوع شدید آن موسوم به گال پوستهدار (Crusted Scabies)، میتواند منجر به بروز عفونتهای باکتریایی ثانویه، عوارض کلیوی، و افزایش خطر ابتلا به بیماریهای التهابی مزمن شود. از این رو، تشخیص دقیق، درمان مؤثر، و اجرای سیاستهای پیشگیرانه برای کنترل و حذف آن از جمعیتهای در معرض خطر، ضرورت دارد.
هدف این مقاله بررسی جامع جنبههای ایمنیشناسی و پاتولوژیکی بیماری گال با تمرکز بر پاسخ ایمنی میزبان، راهکارهای فرار انگل از سیستم ایمنی، و تغییرات بافتی ناشی از آلودگی است. همچنین، تلاش شده است تا با نگاهی به یافتههای نوین در حوزههای ایمنیشناسی مولکولی، پاتوفیزیولوژی و درمانهای نوین، چشماندازی از آینده مدیریت این بیماری ارائه گردد. این بررسی میتواند به متخصصان پوست، ایمونولوژی، و بهداشت عمومی در جهت بهبود راهکارهای درمانی و سیاستگذاریهای بهداشتی کمک شایانی نماید.
عامل بیماریزا: کنه Sarcoptes scabiei
طبقهبندی و گونههای مختلف
کنه Sarcoptes scabiei از راسته Acarina، زیرراسته Astigmata و خانواده Sarcoptidae محسوب میشود. گونههای متعددی از این کنه وجود دارند که هر کدام بهطور اختصاصی میزبان خاصی دارند. در انسان، فرم اختصاصی با عنوان Sarcoptes scabiei var. hominis شناخته میشود. گونههای دیگر این انگل مانند S. scabiei var. canis در سگ و var. suis در خوک دیده میشوند. با وجود تمایل به میزبان خاص، انتقال متقاطع بین گونهها در شرایط خاص ممکن است، هرچند این انتقالات اغلب پایدار نبوده و انگل قادر به تداوم چرخه زندگی خود در میزبان جدید نیست.
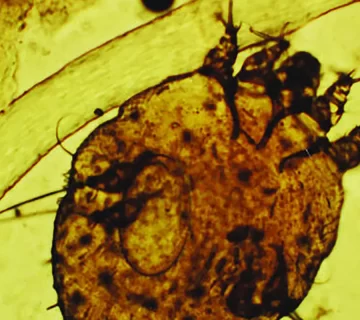
ویژگیهای مورفولوژیک کنه
Sarcpotes scabiei یک کنه میکروسکوپی، بیرنگ و بیبال است که اندازه آن در فرم بالغ بین ۰.۳ تا ۰.۵ میلیمتر متغیر است. بدن این کنه گرد، کوتاه و دارای چهار جفت پا میباشد که به طور اختصاصی برای حرکت در لایههای سطحی پوست طراحی شدهاند. کنه ماده نسبت به نر بزرگتر بوده و نقش اصلی را در ایجاد آلودگی ایفا میکند. سطح بدن انگل دارای خارها و زوائد شاخی است که در نفوذ به پوست و حرکت در اپیدرم نقش دارند. پاهای جلویی مجهز به بادکشهایی است که موجب چسبندگی به بستر پوست میشود.
چرخه زندگی و بقا در خارج از بدن میزبان
چرخه زندگی Sarcoptes scabiei شامل چهار مرحله تخم، لارو، پوره و بالغ است. ماده بالغ پس از جفتگیری با نر، در لایه شاخی پوست تونلهایی ایجاد میکند و روزانه بین ۲ تا ۳ تخم در آن قرار میدهد. تخمها طی ۳ تا ۴ روز به لارو تبدیل شده و سپس از مراحل پورهای عبور کرده و به فرم بالغ میرسند. کل چرخه زندگی حدود ۱۰ تا ۱۴ روز طول میکشد.
در خارج از بدن انسان، این انگل تنها بین ۲۴ تا ۳۶ ساعت در شرایط محیطی زنده میماند، مگر آنکه در محیطهایی با دمای پایین و رطوبت بالا قرار گیرد، که در این حالت میتواند تا ۵ روز نیز زنده بماند. این ویژگی باعث میشود انتقال از طریق وسایل آلوده مانند لباس، ملافه یا مبلمان در موارد خاص بهویژه در گال پوستهدار، امکانپذیر باشد.
مکانیسم نفوذ، تغذیه و تعامل با اپیدرم
پس از تماس با پوست میزبان، کنه ماده بهسرعت به لایه شاخی نفوذ کرده و با ترشح آنزیمها و مواد مخاطی، تونلی برای حرکت و تخمریزی ایجاد میکند. این تونلها محل زیست و تغذیه انگل هستند. تغذیه عمدتاً از طریق جذب مواد کراتینه و سلولهای اپیدرمی انجام میشود. در حین این فرآیند، مواد دفعی، آنتیژنهای سطحی و ترکیبات مترشحه از کنه با بافت میزبان واکنش داده و موجب القای پاسخهای ایمنی و التهابی میشوند. این پاسخها منشأ علائم بالینی بیماری از جمله خارش و ضایعات پوستی هستند.
تعامل کنه با اپیدرم نه تنها موجب تخریب ساختاری پوست میشود، بلکه با تحریک کراتینوسیتها، فیبروبلاستها و سلولهای ایمنی ذاتی مانند ماکروفاژها و ماستسلها، مسیرهای التهابی مختلفی فعال میشود که در بروز بیماری و تداوم علائم نقش دارند.
اپیدمیولوژی بیماری گال
شیوع جهانی و عوامل مستعدکننده
بیماری گال یکی از مشکلات شایع بهداشت عمومی در سراسر جهان است که میلیونها نفر را بهویژه در مناطق پرجمعیت، محروم و با زیرساختهای بهداشتی ضعیف مبتلا میسازد. برآوردهای سازمان جهانی بهداشت نشان میدهد که سالانه بین ۱۵۰ تا ۲۰۰ میلیون نفر در سراسر جهان به این بیماری مبتلا میشوند. گال در تمامی گروههای سنی مشاهده میشود، اما در کودکان، سالمندان، و افرادی با ایمنی ضعیف شایعتر است.
عوامل متعددی در افزایش خطر ابتلا به این بیماری نقش دارند. از جمله این عوامل میتوان به تماس نزدیک و مکرر پوست با پوست، کمبود امکانات بهداشتی، تراکم جمعیت، و تأخیر در تشخیص و درمان اشاره کرد. همچنین، زندگی در محیطهایی مانند کمپهای پناهندگان، خانههای سالمندان، زندانها و خوابگاهها، از جمله موقعیتهایی هستند که خطر انتقال را افزایش میدهند.
نقش شرایط جوی، فقر، تراکم جمعیت
شرایط محیطی و اجتماعی نقش بارزی در شیوع و انتقال گال ایفا میکنند. در مناطق گرمسیری و مرطوب که تعریق و تماس پوستی افزایش مییابد، احتمال انتقال بیشتر است. از سوی دیگر، در مناطق خشک و سرد، بقا و فعالیت انگل در خارج از بدن کاهش مییابد، هرچند شرایط اجتماعی همچنان نقش مهمتری در کنترل بیماری دارد.
فقر یکی از مؤثرترین عوامل در شیوع بالای گال محسوب میشود. کمبود منابع مالی برای خرید دارو، نبود امکانات درمانی مناسب، و ضعف در برنامههای آموزشی و پیشگیری، از جمله پیامدهای فقر هستند که در ایجاد و تداوم بیماری نقش دارند. تراکم جمعیت، بهویژه در خانههای کوچک با تعداد بالای ساکن، احتمال تماس مستقیم پوست به پوست را افزایش داده و شرایط را برای گسترش سریع بیماری فراهم میکند.
الگوهای انتقال در کشورهای توسعهیافته و در حال توسعه
الگوی انتقال بیماری در کشورهای مختلف بسته به سطح توسعهیافتگی و ساختار بهداشتی تفاوت دارد. در کشورهای توسعهیافته، گال بیشتر بهصورت موارد پراکنده (اسپورادیک) یا شیوع محدود در مراکز مراقبت طولانیمدت مانند خانههای سالمندان یا بیمارستانها دیده میشود. در این کشورها، تشخیص زودهنگام، دسترسی به درمانهای استاندارد، و اطلاعرسانی گسترده موجب کاهش شیوع بیماری شده است.
در مقابل، در کشورهای در حال توسعه، گال اغلب بهصورت اندمیک و با شیوع بالا در جمعیتهای عمومی مشاهده میشود. عدم دسترسی به داروهای مؤثر، فقدان برنامههای پیشگیرانه گسترده، و نبود اطلاعات بهداشتی کافی از مهمترین چالشهای این کشورهاست. همچنین، در این کشورها موارد گال پوستهدار بیشتر دیده میشود که به دلیل بار بالای انگل، نقش مهمی در انتقال سریع و گسترده بیماری دارد.
در مجموع، کنترل مؤثر گال نیازمند درک دقیق از الگوهای اپیدمیولوژیک، تعیین گروههای پرخطر، و طراحی مداخلات مناسب متناسب با شرایط هر منطقه است.
پاسخ ایمنی میزبان در برابر کنه گال
پاسخ ایمنی میزبان در برابر آلودگی به Sarcoptes scabiei حاصل تعامل پیچیدهای میان ایمنی ذاتی و اکتسابی است. این پاسخ نقش تعیینکنندهای در شدت بالینی بیماری، بروز علائم، و پیشرفت یا مهار عفونت ایفا میکند. درک عمیق از اجزای ایمنی درگیر، برای طراحی درمانهای هدفمند و پیشبینی واکنش میزبان ضروری است.
ایمنی ذاتی
پاسخ ایمنی ذاتی نخستین خط دفاعی در برابر آلودگی به کنه گال محسوب میشود. این پاسخ توسط سلولهای ایمنی مقیم در پوست و سلولهای التهابی مهاجر تنظیم میشود.
ائوزینوفیلها بهعنوان سلولهای کلیدی در مقابله با انگلها در بافتهای سطحی نقش دارند. افزایش تجمع ائوزینوفیلها در ضایعات پوستی بیماران مبتلا به گال، بهویژه در نوع شدید آن (گال پوستهدار)، بهوفور گزارش شده است. این سلولها با ترشح آنزیمهای سیتوتوکسیک مانند ماژور بیسیک پروتئین (MBP) و پروتئین کاتیونی ائوزینوفیلی (ECP) موجب آسیب به سلولهای انگلی میشوند، اما در عین حال ممکن است به بافتهای میزبان نیز آسیب وارد کنند.
ماستسلها نیز از طریق ترشح هیستامین، تریپتاز و سایر واسطههای شیمیایی نقش عمدهای در القای خارش و التهاب موضعی دارند. این سلولها بهویژه در مراحل اولیه پاسخ به آنتیژنهای انگلی فعال میشوند.
ماکروفاژها بهعنوان سلولهای فاگوسیتکننده نقش دوگانهای در حذف اجزای انگلی و تنظیم التهاب دارند. فعالسازی آنها منجر به ترشح سایتوکاینهایی نظیر IL-1β و TNF-α میشود که در ایجاد التهاب موضعی و فراخوانی سایر سلولهای ایمنی نقش دارند.
سیستم مکمل و واسطههای التهابی
سیستم مکمل از دیگر اجزای مهم ایمنی ذاتی است که در پاسخ به آلودگی با Sarcoptes scabiei فعال میشود. مسیر کلاسیک و جایگزین مکمل میتوانند با کمک به اپسونیزاسیون و لیز انگل نقش مستقیم در پاکسازی آن داشته باشند. با این حال، برخی از اجزای مترشحه از کنه توانایی مهار عملکرد مؤثر مکمل را دارند که این امر به بقای طولانیتر انگل در پوست منجر میشود.
در پاسخ التهابی، سایتوکاینهایی نظیر IL-1β، IL-6، TNF-α، و فاکتورهای شیمیایی نظیر IL-8 و MCP-1 نقش اساسی در فراخوانی و فعالسازی سلولهای التهابی ایفا میکنند. این مولکولها نهتنها در ایجاد التهاب نقش دارند بلکه در بروز علائم بالینی مانند خارش، قرمزی و تورم نیز مؤثر هستند.
ایمنی اکتسابی
پاسخ ایمنی اکتسابی عمدتاً توسط لنفوسیتهای T کمککننده تنظیم میشود و نوع آن بستگی به شدت آلودگی و نوع بالینی گال دارد. در بیماران مبتلا به گال معمولی، تمایل به پاسخ ایمنی نوع Th1 مشاهده میشود که با ترشح IFN-γ، IL-2 و IL-12 همراه است. این نوع پاسخ موجب تقویت ایمنی سلولی و کنترل مؤثرتر انگل میشود.
در مقابل، در بیماران مبتلا به گال پوستهدار، پاسخ ایمنی عمدتاً بهسمت الگوی Th2 سوق پیدا میکند که با افزایش تولید IL-4، IL-5، IL-13 و سطوح بالای IgE همراه است. این الگو سبب پاسخ ایمنی ناکارآمد، التهاب گسترده و تجمع بالای انگل در پوست میگردد.
نقش سلولهای Treg و Th17
سلولهای T تنظیمی (Treg) با ترشح IL-10 و TGF-β نقش مهارکننده در پاسخ ایمنی دارند. افزایش فعالیت این سلولها در بیماران مبتلا به گال پوستهدار میتواند یکی از عوامل سرکوب پاسخ مؤثر ضدانگلی باشد. مطالعات نشان دادهاند که غلبه پاسخ Treg در این بیماران با تحمل ایمنی میزبان نسبت به حضور مزمن انگل همراه است.
در مقابل، سلولهای Th17 با تولید IL-17 و IL-22 نقش مهمی در التهاب پوست، القای پاسخ ضدباکتریایی و حفظ سد اپیدرمی دارند. هرچند نقش دقیق آنها در گال هنوز بهطور کامل مشخص نشده، اما بهنظر میرسد فعالیت آنها در گال معمولی بیشتر از گال پوستهدار باشد و ممکن است در کنترل نسبی عفونت مؤثر باشند.
پاتوفیزیولوژی بیماری گال
پاتوفیزیولوژی گال بازتابی از تعامل پیچیده میان عوامل انگلی، پاسخ ایمنی میزبان و التهاب موضعی و سیستمیک است. شدت و نوع پاسخ ایمنی نقش تعیینکنندهای در تظاهرات بالینی، میزان خارش، گسترش ضایعات و بروز آسیبهای ثانویه دارد. ویژگی اصلی این بیماری، ایجاد خارش شدید، ضایعات التهابی و در مواردی پاسخهای ایمنی ناکارآمد است که به گسترش و مزمن شدن بیماری منجر میشود.
مسیرهای مولکولی التهاب و خارش
خارش در گال نتیجه تحریک پایانههای عصبی پوست به واسطه ترکیبی از عوامل انگلی و واسطههای التهابی است. مطالعات نشان دادهاند که حضور کنه و مواد مترشحه آن مانند پروتئازها، آنزیمهای گوارشی، و آنتیژنهای سطحی، موجب فعالسازی کراتینوسیتها و سلولهای ایمنی مقیم در پوست میشود. این فعالسازی باعث ترشح سایتوکاینها، کموکاینها و نوروپپتیدهایی مانند substance P و nerve growth factor (NGF) میشود که مستقیماً در فعالسازی مسیرهای عصبی خارش نقش دارند.
همچنین، فعالسازی ماستسلها و ائوزینوفیلها منجر به آزادسازی هیستامین و سایر واسطههای خارشزا میشود. این ترکیبات با افزایش نفوذپذیری عروق، افزایش التهاب موضعی و تحریک اعصاب محیطی، زمینهساز خارش شدید و مداوم در بیماران مبتلا به گال هستند.
نقش IL-1β، TNF-α، IL-4، و IgE
واسطههای ایمنی نقش محوری در بروز و تداوم التهاب در گال ایفا میکنند. در فاز حاد بیماری، سایتوکاینهای پیشالتهابی از جمله IL-1β و TNF-α از سوی کراتینوسیتها و ماکروفاژها ترشح میشوند و باعث فعالسازی سایر سلولهای التهابی و افزایش بیان مولکولهای چسبندگی میگردند. این فرآیند موجب تجمع سلولهای ایمنی در محل عفونت و تشدید التهاب پوستی میشود.
در نوع شدید گال، بهویژه در گال پوستهدار، الگوی ایمنی به سمت پاسخ Th2 تغییر مییابد. IL-4 یکی از سایتوکاینهای کلیدی در این مسیر است که موجب تحریک تولید IgE توسط لنفوسیتهای B و افزایش تکثیر ائوزینوفیلها میشود. سطح سرمی IgE در بیماران مبتلا به گال پوستهدار به طور قابل توجهی افزایش مییابد و این موضوع با افزایش حساسیت بافتی، خارش بیشتر و پاسخهای التهابی گسترده مرتبط است.
مکانیسمهای تخریبی سلولی توسط سلولهای CD8+
سلولهای T سیتوتوکسیک (CD8+) نقش مهمی در تخریب سلولهای آلوده به کنه یا سلولهایی که آنتیژنهای انگلی را ارائه میدهند ایفا میکنند. در ضایعات پوستی بیماران مبتلا به گال، بهویژه در نوع ندولی یا مزمن، نفوذ گسترده سلولهای CD8+ مشاهده شده است. این سلولها با ترشح گرانزیم B و perforin باعث القای آپوپتوز در سلولهای اپیدرمی میشوند.
هرچند این مکانیسم برای حذف سلولهای آلوده ضروری است، اما در مواردی با تخریب بیش از حد بافتی، منجر به مزمن شدن التهاب، زخمهای پوستی و بروز ندولهای مقاوم میشود. در گال پوستهدار، ضعف در عملکرد این سلولها و افزایش Treg ممکن است موجب ناتوانی در حذف مؤثر انگل شود.
اثرات سیستمیک بالقوه در موارد شدید
در موارد شدید بیماری، بهویژه در گال پوستهدار که بار انگلی بسیار بالاست، پاسخ ایمنی میزبان میتواند از سطح موضعی فراتر رفته و اثرات سیستمیک بهدنبال داشته باشد. سطح بالای سایتوکاینهای پیشالتهابی در خون، از جمله IL-6، IL-1β و TNF-α، میتواند موجب بروز تب، لنفادنوپاتی، و پاسخهای التهابی سیستمیک شود.
در مطالعات حیوانی، شواهدی از درگیری کبد، کلیه، و طحال در اثر تحریک مزمن ایمنی و استرس اکسیداتیو مشاهده شده است. این یافتهها نشان میدهند که در صورت عدم درمان مؤثر، گال میتواند نهتنها به تخریب شدید پوستی منجر شود، بلکه موجب اختلال در عملکرد اندامهای داخلی و افزایش خطر ابتلا به بیماریهای التهابی مزمن گردد.
راههای فرار انگل از پاسخ ایمنی میزبان
کنه Sarcoptes scabiei در طول تکامل خود توانسته است راهکارهای متعددی برای گریز از پاسخ ایمنی میزبان توسعه دهد. این استراتژیها به انگل اجازه میدهند که در لایه شاخی پوست باقی بماند، تکثیر کند و علیرغم فعالسازی پاسخهای ایمنی موضعی و سیستمیک، از حذف مؤثر توسط سیستم ایمنی میزبان مصون بماند. این توانایی در فرار از ایمنی، نقش مهمی در تداوم آلودگی، مزمن شدن بیماری و شیوع بالای آن در جمعیتهای انسانی دارد.
مهار سیتوکینهای پیشالتهابی
یکی از مکانیسمهای اصلی فرار ایمنی در Sarcoptes scabiei، سرکوب ترشح و فعالیت سایتوکاینهای پیشالتهابی بهویژه IL-8 است. IL-8 یک کموکاین کلیدی در جذب نوتروفیلها به محل عفونت است و نقش مهمی در آغاز التهاب حاد ایفا میکند. مطالعات نشان دادهاند که پروتئینهای مترشحه از کنه میتوانند تولید IL-8 در کراتینوسیتها را مهار کرده و در نتیجه پاسخ التهابی اولیه را تضعیف نمایند. این مهار باعث تأخیر در شناسایی انگل و کاهش نفوذ سلولهای التهابی به محل نفوذ میشود.
تولید مهارکنندههای پروتئاز و سرکوب مسیر مکمل
بسیاری از پروتئینهای مترشحه توسط Sarcoptes scabiei دارای فعالیت مهارکنندگی بر مسیرهای آنزیمی کلیدی سیستم ایمنی هستند. از جمله این ترکیبات میتوان به مهارکنندههای پروتئاز اشاره کرد که با تداخل در عملکرد پروتئازهای سرمی و سلولی، مسیرهای التهابی را محدود میسازند. این مهارکنندهها میتوانند با مهار کاسکادهای تجزیه پروتئینی در مسیرهای مکمل، از فعالسازی مؤثر سیستم مکمل جلوگیری کرده و مانع از اپسونیزاسیون و لیز مستقیم انگل شوند.
کاهش بیان مولکولهای چسبندگی سلولی
پروتئینهای سطحی و ترشحی کنه همچنین میتوانند باعث کاهش بیان مولکولهای چسبندگی سلولی مانند ICAM-1 و VCAM-1 بر سطح کراتینوسیتها و سلولهای اندوتلیال شوند. این مولکولها در فرآیند اتصال و نفوذ سلولهای ایمنی به بافت آسیبدیده نقش دارند. کاهش بیان آنها باعث اختلال در مهاجرت و تجمع مؤثر سلولهای ایمنی در محل آلودگی شده و به کنه اجازه میدهد مدت طولانیتری در پوست باقی بماند.
القای IL-10 و IL-1ra برای تعدیل پاسخ التهابی
کنه گال قادر است با تحریک کراتینوسیتها و سلولهای ایمنی میزبان، ترشح سایتوکاینهای ضدالتهابی مانند IL-10 و گیرنده آنتاگونیست IL-1 (IL-1ra) را افزایش دهد. IL-10 بهعنوان یک سایتوکاین تعدیلکننده قوی، فعالیت سلولهای T کمککننده، ماکروفاژها و سلولهای دندریتیک را مهار کرده و منجر به کاهش تولید سایتوکاینهای پیشالتهابی و مهار پاسخ ایمنی مؤثر میشود. بهعلاوه، IL-1ra با مهار گیرندههای IL-1 از بروز اثرات التهابی این سایتوکاین جلوگیری میکند.
افزایش بیان این ترکیبات ضدالتهابی بهویژه در بیماران مبتلا به گال پوستهدار دیده میشود و ممکن است یکی از عوامل اصلی ناتوانی سیستم ایمنی در پاکسازی انگل و افزایش بار انگلی باشد. این فرآیندها در مجموع یک محیط ایمنی مهارشده ایجاد میکنند که بقای طولانیمدت انگل را در پوست تسهیل مینماید.
عوارض و عفونتهای ثانویه
گرچه بیماری گال بهصورت اولیه محدود به لایههای سطحی پوست و واکنشهای موضعی است، اما در بسیاری از موارد، بهویژه در شرایط تأخیر در درمان یا در جمعیتهای آسیبپذیر، میتواند منجر به بروز عوارض جدی ثانویه شود. این عوارض نهتنها سلامت جسمی، بلکه وضعیت روانی، اجتماعی و کیفیت زندگی فرد مبتلا را نیز تحت تأثیر قرار میدهند. در این میان، عفونتهای باکتریایی پوست از جمله پیامدهای بالینی مهم گال هستند که میتوانند به بروز بیماریهای سیستمیک و مزمن بیانجامند.
نقش استافیلوکوک و استرپتوکوک گروه A
خارش شدید ناشی از گال و خاراندن مکرر پوست منجر به ایجاد زخمهای سطحی و تخریب سد دفاعی اپیدرم میشود. این شرایط فرصت مناسبی برای ورود عوامل باکتریایی به لایههای عمقیتر پوست فراهم میسازد. در این میان، دو باکتری Staphylococcus aureus و Streptococcus pyogenes (گروه A) نقش اصلی در عفونتهای ثانویه ناشی از گال دارند.
عفونتهای باکتریایی ثانویه میتوانند به اشکال مختلفی از جمله امپتیگو، سلولیت، فولیکولیت و آبسههای پوستی ظاهر شوند. در برخی بیماران، بهویژه کودکان، کلونیزاسیون مزمن با استرپتوکوک گروه A میتواند زمینهساز بروز بیماریهای سیستمیک با منشأ ایمنی شود که عوارض درازمدتی به دنبال دارند.
نارسایی کلیوی و تب روماتیسمی به دنبال عفونتهای پوستی
یکی از مهمترین پیامدهای عفونتهای استرپتوکوکی پوست، گلومرولونفریت حاد پس از استرپتوکوک (post-streptococcal glomerulonephritis) است. در این وضعیت، آنتیژنهای استرپتوکوکی در کلیه تهنشین شده و باعث فعالسازی سیستم ایمنی و التهاب گلومرولی میشوند. این بیماری میتواند به صورت حاد یا مزمن بروز کرده و در مواردی منجر به نارسایی کلیه شود.
همچنین، تب روماتیسمی حاد یکی دیگر از عوارض بالقوه عفونتهای استرپتوکوکی پوست است. اگرچه این بیماری بیشتر بهدنبال عفونتهای حلقی مشاهده میشود، اما در مناطق گرمسیری و منابع محدود، شواهدی از ارتباط آن با عفونتهای پوستی نیز گزارش شده است. تب روماتیسمی با درگیری مفاصل، قلب و سیستم عصبی مرکزی همراه است و میتواند منجر به بیماری قلبی روماتیسمی در سنین جوانی شود.
عوارض روانی و اجتماعی بهویژه در کودکان و جوامع محروم
اثرات گال محدود به مشکلات فیزیکی نیست، بلکه جنبههای روانی و اجتماعی قابل توجهی نیز دارد. خارش مداوم، بیخوابی، احساس شرم و طرد اجتماعی از جمله عواملی هستند که کیفیت زندگی بیماران را بهویژه در کودکان و نوجوانان بهشدت کاهش میدهند. کودکان مبتلا به گال ممکن است از طرف همکلاسیها مورد تمسخر یا طرد قرار گیرند که این امر منجر به انزوای اجتماعی، افت تحصیلی و اختلالات روانی میشود.
در جوامع محروم، گال اغلب با انگ اجتماعی همراه است و ممکن است بهعنوان نمادی از فقر و بیتوجهی تلقی شود. این نگرش منفی میتواند موجب پنهانکاری بیماران، تأخیر در مراجعه به مراکز درمانی، و تداوم زنجیره انتقال بیماری شود. از اینرو، ارتقاء سطح آگاهی عمومی، کاهش برچسبهای اجتماعی و حمایت روانی از بیماران از اجزای مهم در کنترل و مدیریت مؤثر این بیماری محسوب میشود.
تغییرات بافتشناسی گال
بررسی بافتشناسی ضایعات پوستی در بیماران مبتلا به گال، اطلاعات ارزشمندی در خصوص پاتوفیزیولوژی و شدت بیماری فراهم میکند. بسته به نوع بالینی گال، ویژگیهای آسیبشناسی متغیر بوده و نمای میکروسکوپی میتواند به افتراق انواع گوناگون بیماری و نیز افتراق آن از سایر درماتوزهای التهابی کمک کند.
تفاوتهای پاتولوژیک بین گال معمولی، ندولی، تاولی و پوستهپوسته
در گال معمولی، نمای بافتی معمولاً شامل هیپرکراتوز خفیف، اسپونژوزیس، و ارتشاح مختصر سلولهای التهابی در درم است. ضایعات غالباً در اپیدرم محدود باقی میمانند و واکنشهای ایمنی شدید مشاهده نمیشود.
در گال ندولی (nodular scabies) که اغلب در نواحی تناسلی یا زیر بغل دیده میشود، گرههای التهابی مقاوم با نفوذ گسترده لنفوسیتها، ائوزینوفیلها و ماستسلها در درم مشاهده میشود. در برخی موارد، ساختارهایی شبیه گرانولوم تشکیل میشود که بهواسطه پاسخ ایمنی مزمن و باقیماندن اجزای کنه در بافت ایجاد شدهاند.
در گال تاولی (bullous scabies) که کمتر شایع است، تشکیل وزیکول یا بول در اپیدرم دیده میشود. نمای میکروسکوپی ممکن است شبیه به پمفیگوس یا بیماریهای تاولی خودایمنی باشد. پاسخ ایمنی در این حالت بهویژه با مشارکت نوتروفیلها در لایههای اپیدرمی همراه است.
در گال پوستهپوسته (crusted scabies) که شدیدترین نوع بیماری محسوب میشود، لایه شاخی دچار هیپرکراتوز شدید، پاراناکراتوز و تجمع وسیع انگل، تخم و مدفوع آن است. در این حالت، تعداد زیادی از کنهها در زیر لایه شاخی مشاهده میشوند و نفوذ گسترده سلولهای التهابی در درم عمقی دیده میشود. پاسخ ایمنی در این حالت اغلب ناکارآمد و بهسمت سرکوب ایمنی سوق یافته است.
بررسی آسیبشناسی در نواحی مختلف پوست
شدت و نوع پاسخ التهابی ممکن است بسته به محل ضایعه در بدن متفاوت باشد. نواحی با پوست نازکتر مانند فضای بین انگشتان، نواحی تناسلی و چینهای بدن معمولاً با ارتشاح التهابی بیشتر و تخریب وسیعتری همراهاند. در مقابل، در نواحی با پوست ضخیمتر مانند کف دست یا پا، هیپرکراتوز شدیدتر و ضخامت لایه شاخی بارزتر است.
در نواحی مزمن، بهویژه در محل گالهای درماننشده یا مکرر، تغییراتی مانند آکانتوز، فیبروز خفیف در درم، و نئوواسکولاریزاسیون نیز ممکن است مشاهده شود که نشاندهنده تداوم التهاب و بازسازی مزمن بافتی هستند.
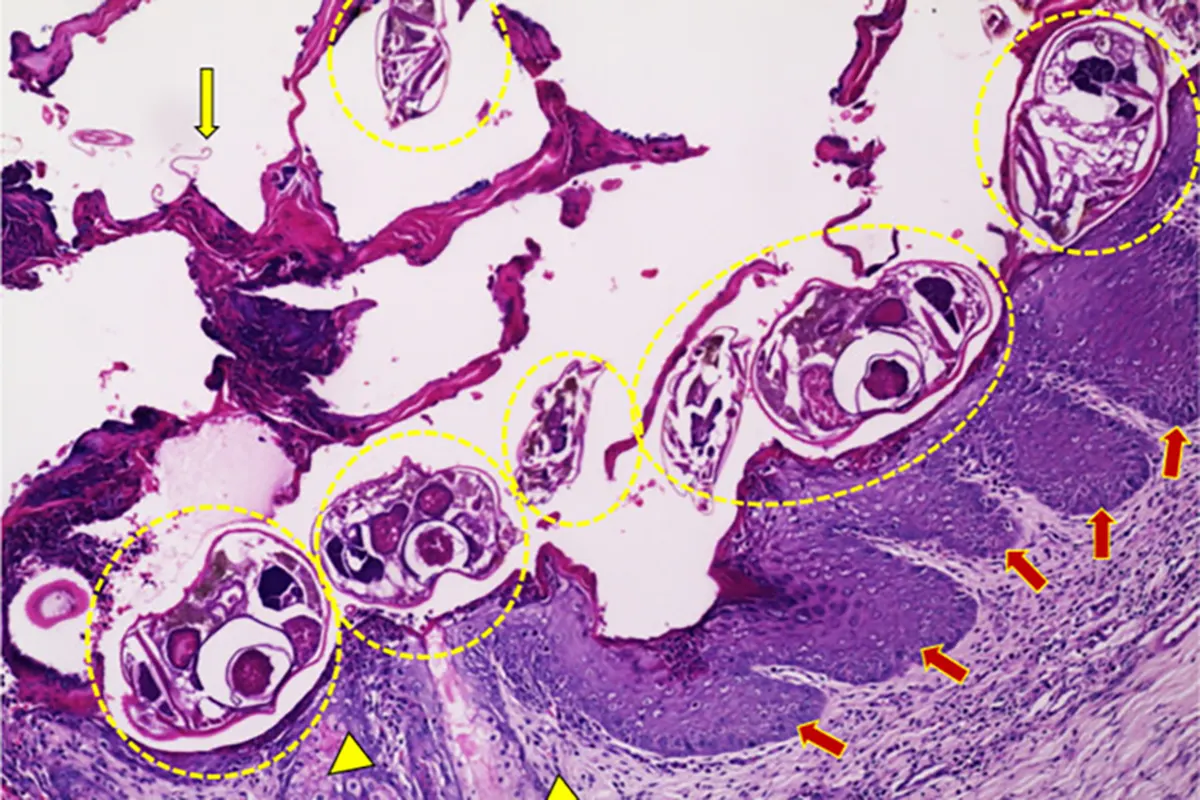
یافتههای میکروسکوپی
بررسی میکروسکوپی ضایعات پوستی در بیماران مبتلا به گال معمولاً شامل یافتههای زیر است:
- تونلهای حفر شده توسط انگل در لایه شاخی پوست (stratum corneum)، که ممکن است حاوی کنه بالغ، تخم یا مدفوع انگل باشد.
- هیپرکراتوز، بهویژه در گال پوستهپوسته، که بهصورت ضخیمشدن لایه شاخی نمایان میشود.
- گرانولومهای لنفوسیتی یا ائوزینوفیلیک، بهویژه در گال ندولی.
- نفوذ سلولهای التهابی شامل لنفوسیتها، ماکروفاژها، ائوزینوفیلها و گاه نوتروفیلها در درم.
- اسپونژوزیس و آکانتوز بهعنوان واکنشهای التهابی اپیدرمی.
یافتههای فوق میتوانند بسته به مرحله بیماری، پاسخ ایمنی میزبان و وجود یا عدم وجود درمان قبلی متفاوت باشند. استفاده از تکنیکهای رنگآمیزی اختصاصی، مانند PAS یا Giemsa، ممکن است به تشخیص بهتر ساختارهای انگلی و افتراق آنها از آرتیفکتهای اپیدرمی کمک کند.
درگیری سیستمیک در موارد شدید
اگرچه گال در اغلب موارد به لایههای سطحی پوست محدود میماند، اما در نوع شدید و مزمن آن، بهویژه گال پوستهپوسته، شواهدی از تأثیرات سیستمیک و درگیری اندامهای داخلی گزارش شده است. این موارد عمدتاً در مدلهای حیوانی بررسی شدهاند و میتوانند نمایانگر مسیرهای بالقوه آسیب در انسان نیز باشند.
تغییرات کبدی، کلیوی، قلبی و طحال در مطالعات حیوانی
مطالعات تجربی در حیوانات آلوده به Sarcoptes scabiei، بهویژه در خرگوش و خوکچههندی، نشان دادهاند که آلودگی شدید با انگل میتواند منجر به تغییرات پاتولوژیک در اندامهایی مانند کبد، کلیه، قلب و طحال شود. در بافت کبد، افزایش نفوذ سلولهای التهابی، نکروز نقطهای، و اختلال در ساختار پارانشیمی گزارش شده است. در کلیه، گاهی گلومرولونفریت، نفوذ سلولهای مونونوکلئر و افزایش بیان مولکولهای التهابی مشاهده شده است.
در قلب، تغییراتی مانند دژنراسیون فیبرهای عضلانی و افزایش ارتشاح لنفوسیتی در اطراف عروق ثبت شدهاند که ممکن است نتیجه پاسخ ایمنی سیستمیک مزمن باشند. در طحال نیز، هایپرپلازی فولیکولهای لنفاوی و بزرگشدن اندام گزارش شده که حاکی از فعالسازی مزمن ایمنی و تلاش بدن برای کنترل عفونت است.
نقش استرس اکسیداتیو و سیتوکینها در درگیری اندامهای داخلی
استرس اکسیداتیو و افزایش سطح سیتوکینهای پیشالتهابی در جریان خون، از عوامل مهمی هستند که در بروز آسیبهای سیستمیک در آلودگی شدید به گال نقش دارند. مطالعات نشان دادهاند که در این شرایط، تعادل بین رادیکالهای آزاد و آنتیاکسیدانهای طبیعی بدن بر هم خورده و موجب آسیب به غشاهای سلولی، DNA و آنزیمهای حیاتی میشود.
افزایش سیتوکینهایی مانند TNF-α، IL-1β و IL-6 در سطوح سیستمیک، میتواند باعث القای پاسخ التهابی عمومی، اختلال عملکرد سلولهای اندوتلیال، و در نهایت آسیب به اندامهای حیاتی گردد. این پدیدهها بهویژه در افرادی با ایمنی سرکوبشده، افراد سالمند یا کودکان دچار سوءتغذیه ممکن است پیامدهای بالینی مهمتری بهدنبال داشته باشد.
نتیجهگیری
گال یکی از بیماریهای پوستی مزمن و واگیر است که بهرغم ظاهر نسبتاً ساده و محدود آن، دارای پیچیدگیهای ایمونولوژیک و پاتوفیزیولوژیک قابل توجهی است. شناخت دقیق مکانیسمهای مولکولی بیماری، از جمله تعامل بین کنه و میزبان، مسیرهای فرار ایمنی، نقش واسطههای التهابی و پیامدهای بافتی، برای طراحی درمانهای مؤثر و پایدار ضرورت دارد.
با توجه به شیوع بالا، بار اجتماعی و روانی بیماری، و خطر بروز عوارض ثانویه جدی، توسعه راهبردهای جهانی برای تشخیص زودهنگام، درمان مؤثر، و کنترل اپیدمیولوژیک بیماری ضروری است. این امر نیازمند مشارکت چندسویه میان سازمانهای بهداشتی، محققان، دولتها و جوامع محلی است.
چشمانداز آینده درمان گال امیدوارکننده است. فناوریهای نوین در زمینه ایمنیشناسی، بیوانفورماتیک، ژنومیکس و طراحی دارو، مسیر را برای توسعه واکسنهای بالقوه، داروهای با اثربخشی بالا، و ابزارهای تشخیصی سریع و دقیق هموار کردهاند. سرمایهگذاری در پژوهشهای بنیادی و بالینی در این حوزه میتواند در آیندهای نزدیک به کنترل کامل یا حتی حذف این بیماری از جمعیتهای انسانی منجر شود.

بدون دیدگاه